Попередня сторінка: 38. Kvantumgenerátorok (lézerek)
Наступна сторінка: 40. Radioaktivitás. A radioaktív hasadás alaptörvénye
Képzeljétek magatok elé az első meleg tavaszi napokat, az iskolai nagyszünetet. Alighogy megszólalt a csengő, a gyerekek szétszaladtak az udvaron. Úgy tűnik, nincs erő, ami visz-szatarthatja őket. Első ránézésre a protonoknak a magban az iskolásokhoz hasonlóan kellene viselkedniük - minden irányba „szétszaladni" az elektrosztatikus taszítási erők hatására, a magnak pedig szét kellene hullania. Mivel ez nem történik meg, ezért logikusan arra a következtetésre juthatunk, hogy létezik valamilyen erő, amely a nukleonokat összetartja. Vajon mi ez az erő?
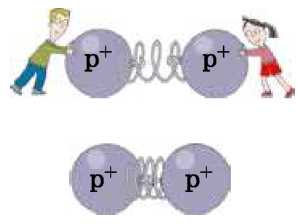
Felidézzük az atom felépítését
Az atommagot kétféle részecske alkotja: pozitív töltéssel rendelkező protonok és negatív töltésű neutronok. A proton tömege 1800-szor nagyobb a neutron tömegénél.
Az atommagot alkotó protonokat és neutronokat nukleonoknak nevezik (latin nucleus -mag).
Az atomban lévő nukleonok összmennyi-ségét tömegszámnak (nukleonszámnak) nevezzük. Jelölése: A.
Az atom elektromosan semleges: a protonok töltésének értéke az atommagban megegyezik a neutronok töltésének összegével. A proton töltésének abszolút értéke megegyezik az elektron töltésének abszolút értékével (az e = 1,6 · 10-19 C elemi töltéssel), ezért a semleges atomban a protonok és neutronok száma azonos.
Az atommagban lévő proton számát protonszámnak nevezzük. A jele: Z. A protonszám könnyen meghatározható a kémiai elemek Men-gyelejev-fele periódusos rendszerének segítségével, ahol az elem táblázatbeli rendszáma az atommagban lévő protonok számát (protonszámot) jelenti.
Ismerve a kémiai elem Z rendszámát és A tömegszámát, meghatározható a magban lévő neutronok N száma: N - A - Z.
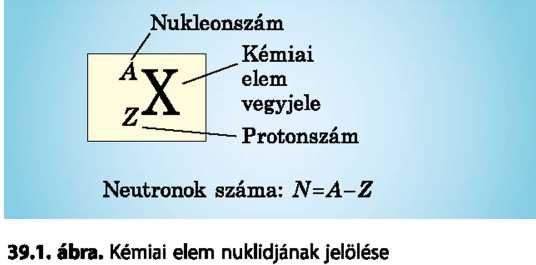
Azt az atomfajtát, amelyet a protonszáma és tömegszáma határoz meg, nuklidnak nevezik (39.1. ábra).
Az atommag tanulmányozásának története
1911. Ernest Rutherford (1871-1937) angol fizikus az a-részecskék szóródásának mérése során felfedezte az atommagot.
1913. Henry Moseley (1887-1915) angol fizikus megmérte az atommag elektromos töltését.
1919. Rutherford a nitrogént α-részecskékkel bombázva felfedezte a p protont - a hidrogénatom magját.
1920. Rutherford különféle elemeket a-részecskékkel bombázva felfedezte, hogy az α-részecskék az elemek magjából szintén protonokat ütnek ki. A tudós azt a következtetést vonta le, hogy az összes elem atomjai protonokat tartalmaznak, és feltételezte annak lehetőségét, hogy az atommagban olyan semleges részecske található, amelynek tömege nagyjából azonos a proton tömegével.
1932. James Chadwick (1891-1974) angol fizikus a berillium a-részecskékkel végzett kísérletek során
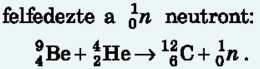
1932. Dmitrij Dmitrijevics Ivanenko (1904-1994) szovjet és Werner Karl Heisenberg (1901—1976) német fizikusok felállították az atommag proton-neutron felépítésének hipotézisét.
(D. D. Ivanenko Poltavá-ban született, Harkivban, Kijevben, Leningrádban (jelenleg Szentpétervár) és Moszkvában dolgozott.)
Ha a különböző nuklidoknak azonos a protonszáma, akkor kémiai tulajdonságaik is azonosak — a nuklidok egy elemhez tartoznak.
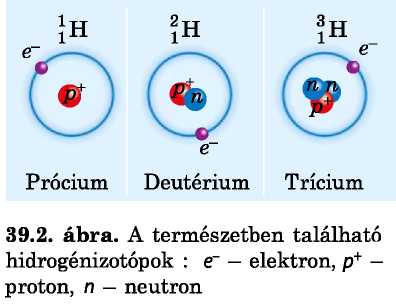
Az izotópok („azonos helyűek") egyazon kémiai elem olyan módosulatai, amelyek atommagjai azonos számú protonból, de eltérő számú neutronból épülnek fel.
Minden kémiai elem több izotóppal rendelkezik (39.2. ábra).
Hány proton és neutron található az urán
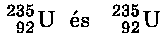
magjaiban?
A magerők alaptulajdonságai
A magok nagyon stabilak. De akkor miképpen lehetséges, hogy egy atomon belül megmaradnak az egymáshoz nagyon közeli protonok, hiszen az egynemű töltések taszítják egymást, a neutronoknak nincs töltésük, a gravitációs erűk pedig 1036-szor kisebbek az elektromágneses taszítóerőknél?
Tisztázott, hogy a nukleonok között erős kölcsönhatás van, amely jelentősen meghaladja az elektromágneses kölcsönhatást. Megjegyezzük, hogy az erős kölcsönhatás - alapkölcsönhatás, amely nem csak a nukleonok kölcsönhatásánál jelenik meg.
Az atommag protonjai és neutronjai között ható és az atommagok létezését biztosító erőket magerőknek (nukleáris erőknek) nevezzük (39.3. ábra).
A nukleáris erők fő tulajdonságai:
1) a természetben előforduló erűk közül a legerősebbek — 100-1000-szer erősebbek két proton között kis távolságokon (~10-15 m) ható elektrosztatikus
taszítóerőnél;
2) kizárólag vonzóerők·
3) rövid hatótávolságúak. A mérések azt mutatták, hogy a nukleonok közötti intenzív kölcsönhatás a nukleon méretével megegyező távolságokon (~10-15 m) történik;
4) bármilyen nukleon között hatnak, nem tesznek különbséget a proton és a neutron között: proton/proton, neutron/neutron, proton/neutron. A nukleáris erűk a felsorolt esetekben egyenlők;
5) tulajdonsága a telítettség·, egy nukleon csak meghatározott számú szomszéddal tud kölcsönhatásba lépni.

Az atommag kötési energiája
A magerők jóval erősebbek a Coulomb-féle erőknél, ezért a mag különálló nukleonokra történő „felosztásához” munkát kell végezni, tehát bizonyos mennyiségű energiát kell elhasználni.
Az atommag kötési energiájának (Fköt) az atommagot alkotó nukleonok teljes elkülönítéséhez szükséges energiát nevezzük.
Az energiamegmaradás törvénye alapján ugyanilyen energiára van szükség a mag létrehozásához. Hogyan számítható ki ez az energia? A feleletet a relativitáselmélet adta meg: a tömeget és energiát Einstein képlete kapcsolja össze:
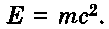
Pontos mérésekkel bebizonyították, hogy a tetszőleges atommag tömege kisebb a magot alkotó nukleonok tömegénél:

ahol mm — a mag tömege; Zmp — a protonok tömege a magban; Nmn — a neutronok tömege a magban.
A magot alkotó nukleonok és az atommag tömegének a különbségét tömeghiánynak (tömegdefektusnak) nevezik:
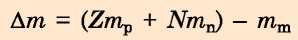
Mivel a mag létrejöttekor a rendszer tömege csökken, a mag létrejötte során felszabaduló energia, tehát a kötési energia is, a következő' képlettel határozható meg:
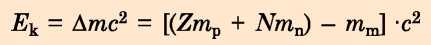
Jegyezzétek meg!
• Az atomfizikában kényelmetlen az Sí rendszerbeli mértékegységeket használni (a részecskék tömege és energiája nagyon kicsi), ezért a részecskék tömegét atomi tömegegységben adják meg (1 a.t.e. = 1,66 0 54 -1027 kg), az energiát pedig megaelektronvoltban (1 MeV = = 1,60222 10-13 J). Egyszerű bebizonyítani: ha
Am = 1 a.t.e., akkor Ek = = 931,5 MeV, tehát:
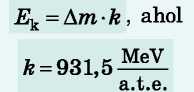
Ha a feladatban a semleges atom tömege van megadva (és nem a mag tömege), akkor az elektronok tömegének figyelembevételével a tömeghiányt a következő' képlettel határozzák meg:
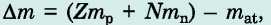
ahol mat — a semleges atom tömege; /nH - az hidrogénatom tömege; mn — a neutron tömege.
Bizonyítsátok be az utolsó egyenletet, figyelembe véve, hogy az elektronok száma a semleges atomban egyenlő a magban lévő protonok számával, az *H hidrogénatom egy protonból és egy elektronból áll!
Az atommag fajlagos kötési energiája
Hogy megértsük, egyes magreakciók miért energiaelnyeléssel mennek végbe, míg mások — energia felszabadulásával, ismernünk kell a fajlagos kötési energiát.
Az atommag f fajlagos kötési energiája - a meghatározott nukleon magját jellemző fizikai mennyiség, amely számszerűleg egyenlő a mag egy nukleonjára eső kötési energiával:
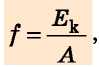
ahol f?k - kötési energia; A — a magban lévő nukleonok száma (tömegszám).
Az f(A) függvény grafikonján három szakasz emelhető ki.
I. szakasz (könnyű magok) — a görbe fokozatosan emelkedik, vagyis a fajlagos kötési energia növekszik; ez azt jelenti, hogy a könnyű magok nehezebbekké történő szintézise (egyesülése) esetén energia szabadul fel.
A II. szakasz (a Periódusos rendszer középső részén lévő elemek atomjai) -szinte egyenes, a görbe csekély maximumot ér el, ami azt jelenti, hogy ennek a résznek az elemei a legstabilabbak.
III. szakasz (nehézmagok) - a fajlagos kötési energia fokozatosan csökken, ezért a magok kevésbé stabilak és osztódásuk esetén energia szabadul fel.
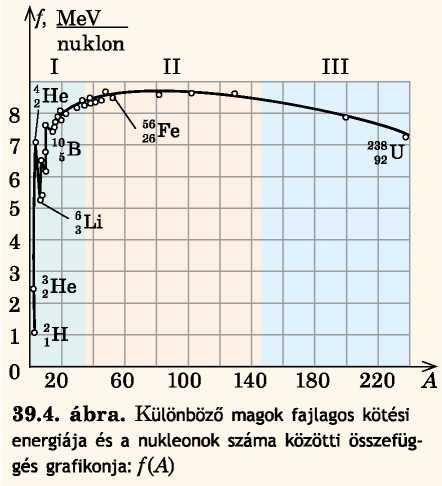
A 39.4. ábrán látható a különböző' magok fajlagos kötési energiája és a nukleonok száma közötti összefüggés, vagyis az f(A) függvény grafikonja. A grafikon elemzésével megtalálhatók azok a módszerek, amelyekkel nukleáris energia hozható létre: az elsó' mód a nehézmagok hasításában rejlik (hasadási reakció), a második — a könnyű magok egyesítésében (szintézis). Mindkét esetben nagyobb fajlagos kötési energiájú magok jönnek létre: az egyik nukleonra nagyobb tömeghiány jut - a megmaradt tömeg energiává alakul át.
Gyakoroljuk a feladatok megoldását!
Feladat. Határozzátok meg a nukleonok fajlagos kötési energiáját a hélium izotóp (2He) magjában! A szükséges adatokat megtaláljátok az 1. függelék
6. táblázatában.
A fizikai probléma elemzése. A hélium 2He magjában 2 proton (Z = 2) és 4 nukleon (A=4) található. A hidrogénatom tömegének, valamint a héliumatom és proton tömegeinek az értéke segítségével megkapjuk az a.t.e.-ben mért tömeghiányt, majd kiszámítjuk a kötési energiát.

Összegezés
Az atommag nukleonokból - protonokból és neutronokból áll. Az adott elem protonszáma (Z) egyenlő a kémiai elemek Mengyelejev-féle periódusos rendszerében lévő rendszámával, a nukleonok száma (A) pedig — a tömegszámmal.
Az izotópok egyazon kémiai elem olyan módosulatai, amelyek atommagjai azonos számú protonból, de eltérő számú neutronból épülnek fel.
Az atommag protonjai és neutronjai a közöttük ható magerőknek köszönhetően maradnak a magban. A magerők közelhatók — a nukleonok méreténél nagyobb távolságon nem észlelhetők.
A magot alkotó nukleonok és az atommag tömegének a különbségét Ám tömeghiánynak nevezzük. A tömeghiány határozza meg a kötési energiát:
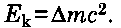
Az atomenergia felszabadulása például könnyű magok fúziója és kemény magok hasadása által jöhet létre.
Ellenőrző kérdések
1. Milyen részecskékből áll az atommag? 2. Hogyan határozható meg a magban lévő protonok és neutronok száma? Mondjatok példákat! 3. Mi a nuklid? 4. Milyen nuklidokat nevezünk izotópoknak? Mondjatok példákat! 5. Milyen kölcsönhatás tartja a nukleonokat az atommagban? 6. Mit nevezünk nukleáris erőknek? Soroljátok fel a tulajdonságait! 7. Mi a tömeghiány, és hogyan határozható meg? 8. Definiáljátok a kötési energia fogalmát! Hogyan számítható ki? 9. Jellemezzétek a fajlagos kötési energiát mint fizikai mennyiséget! 10. Miért szabadul fel energia a könnyű magok fúziója és a kemény magok hasadása során?
39. gyakorlat
1. Határozzátok meg, hány proton és hány neutron található a következő izotópok atommagjában: fluor
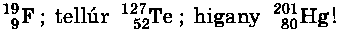
2. Melyik elem magjának nulla a kötési energiája?
3. A fajlagos kötési energia és a tömegszám közötti összefüggés grafikonja alapján (39.4. ábra) határozzátok meg, hogy a 210 nukleonból álló atommag hasadásakor az energia felszabadul vagy elnyelődik?
Határozzátok meg a nitrogén
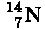
atommagjának tömeghiányát, kötési és
fajlagos kötési energiáját!
Mekkora a fajlagos kötési energiája az oxigén-17 izotóp magjának?
6. Az urán-235 magjának hasadásakor bárium-142 és kripton-91 magok keletkeztek. Mennyi energia szabadult fel eközben? Az urán-235 atommag fajlagos kötési energiája - 7,59 MeV/nukleon, a bárium-142 esetében -8,38 MeV/nukleon, a kripton-91-nél - 8,55 MeV/nukleon.
7. A 39. §. 1. pontjában lévő tudósok listáját tovább folytathatjuk: Irene Joliot-Curie, Lise Meitner, Otto Hahn, Francis William Aston és sokan mások. Az atommag héjmodelljének megalkotásáért Maria Göppert-Mayer 1963-ban fizikai Nobel díjat kapott. Készítsetek rövid (1-2 perces) beszámolót a felsorolt tudósok egyikéről vagy egyikük kutatásáról!
Fizika tankönyv 11. osztályosok szerzők Dovgy, Baryakhtar, Loktev
Наступна сторінка: 40. Radioaktivitás. A radioaktív hasadás alaptörvénye