Попередня сторінка: 20. Решение задач при наличии примесей �...
Наступна сторінка: 22. Жиры
Материал параграфа поможет вам:
- различать эстеры среди других соединений;
- составлять формулы эстеров и называть эти вещества;
- узнать о свойствах и получении эстеров.
Запах многих цветов, плодов, фруктов, ягод обусловлен наличием в них органических веществ определенного класса — эстеров.
Эстеры — производные карбоновых кислот, в молекулах которых атом Гидрогена карбоксильной группы замещен на углеводородный остаток.1
1 Раньше такие соединения называли сложными эфирами.
Общая формула эстеров
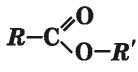
или

Получение. Эстеры образуются при взаимодействии карбоновых кислот со спиртами
(§ 19):
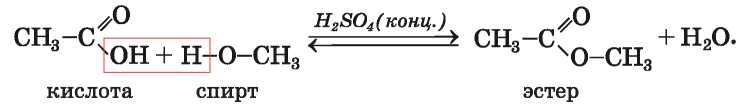
Такие реакции, как вам известно, называют реакциями эстерификации. Они являются обратимыми; одновременно с прямой реакцией протекает обратная — взаимодействие эстера с водой. Чтобы достичь более полного превращения кислоты и спирта в эстер, реакционную смесь нагревают для удаления паров одного из продуктов реакции.

Реакции обмена между веществом и водой называют реакциями гидролиза.
Названия. Систематические названия эстеров состоят из двух частей. Первой частью является название углеводородного остатка в молекуле соответствующего спирта, а второй — название углеводорода, от которого происходит кислота, с суффиксом -оат:

В других названиях эстеров используют название углеводородного остатка молекулы спирта и название карбоновой кислоты (или ее остатка). Например, эстер CH3COOCH3 (рис. 52) называют метиловым эстером уксусной кислоты или метилацетатом.
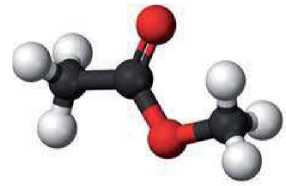
Рис. 52.
Шаростержневая модель молекулы метилэтаноата
Предложите для этилпропаноата другое название и изобразите структурную формулу молекулы соединения.
Свойства. Эстеры с небольшими молекулярными массами являются бесцветными летучими жидкостями преимущественно с приятным запахом. Так, метилбутаноат

(рис. 53). Эстеры с несколькими десятками атомов Карбона в молекулах — твердые вещества, не имеющие запаха.

Рис. 53.
Природные
источники
эстеров
Такие эстеры
входят в состав пчелиного воска (больше всего в нем эстера
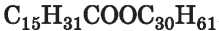
производного
пальмитиновой кислоты).
Молекулы эстеров не содержат гидроксильных групп и не могут образовывать водородные связи. Поэтому эти вещества нерастворимы в воде, но растворяются в органических растворителях.
Эстеры медленно взаимодействуют с водой, т. е. подвергаются гидролизу. При наличии кислот или щелочей1 скорость этой реакции возрастает.
Составьте уравнение реакции гидролиза ме-тилпропаноата.
Это интересно
Ненасыщенный эстер метилметакрилат используют в производстве органического стекла.
Эстеры — горючие вещества.
Применение. Некоторые эстеры карбоновых кислот являются компонентами духов, косметических средств, фруктовых эссенций. Этилацетат и этилформиат служат растворителями для красок и лаков.
ВЫВОДЫ
Эстеры — производные карбоновых кислот, в молекулах которых атом Гидрогена карбоксильной группы замещен на углеводородный остаток. Общая формула эстеров — .K-COOii'. Многие эстеры распространены в природе.
Эстеры с небольшими молекулярными массами являются бесцветными летучими жидкостями, обычно с приятным запахом. Они растворяются в органических растворителях, подвергаются гидролизу, горят. Эстеры образуются при взаимодействии спиртов с карбоновыми кислотами. Их используют в парфюмерии, косметике, в качестве пищевых добавок.
1 В щелочной среде при гидролизе эстера образуется не карбоновая кислота, а ее соль.
154. Найдите соответствие:

155. Найдите соответствие:

156. Из приведенных формул выберите те, которые принадлежат эстерам, и дайте этим веществам систематические названия:
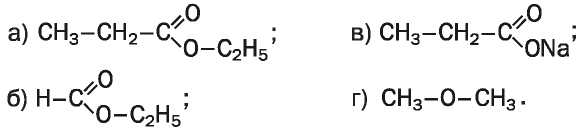
157. Составьте структурные формулы молекул таких эстеров:
а) бутил мета ноата;
б) этил формиата;
в) пропилового эстера муравьиной кислоты.
158. Напишите уравнения реакций:
а) эстерификации с участием пропан-1-ола и этановой кислоты;
б) гидролиза метилпропаноата;
в) горения метил мета н оата.
159. Составьте уравнения реакций, с помощью которых можно осуществить такие превращения:

160. Какая масса метанола была взята для получения метилбутаноата, если образовалось 20,4 г эстера, а прореагировало 80 % спирта?
ДЛЯ ЛЮБОЗНАТЕЛЬНЫХ
Нитроглицерин
Эстеры могут быть образованы не только карбоновыми кислотами, но и неорганическими оксигенсодержащими кислотами. Среди них — эстер глицерола и нитратной кислоты, тривиальное название которого — нитроглицерин. Это соединение используют для изготовления динамита; оно является одним из сильнейших взрывчатых веществ. Промышленное производство нитроглицерина связано с именем шведского изобретателя и предпринимателя А. Нобеля (он основал премию, которую позднее назвали Нобелевской).
Водный раствор нитроглицерина с его массовой долей 1 %, а также таблетки, содержащие это соединение, применяют в медицине как сосудорасширяющее средство.
Нитроглицерин — маслянистая жидкость без запаха. Вещество получают, осуществляя реакцию глицерола со смесью концентрированных нитратной и сульфатной кислот:
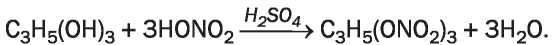
При нагревании или слабом ударе нитроглицерин взрывается:
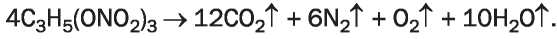
Это материал учебника Химия 10 класс Попель, Крикля
Наступна сторінка: 22. Жиры