Попередня сторінка: Амінокислоти
Наступна сторінка: Високомолекулярні сполуки
Пригадайте: з курсу біології просторову будову молекул білків.
Білки — похідні амінокислот
Білки — природні високомолекулярні сполуки, молекули яких складаються із залишків молекул амінокислот, які сполучені один з одним пеп-тидними зв'язками.
Білки є полімерами, мономерами яких є амінокислоти. Зазвичай білки містять 100 і більше залишків молекул амінокислот. Більшість білків людського організму містять кілька сотень амінокислотних залишків. Отже, молекулярна маса білків коливається від декількох тисяч до декількох мільйонів.
За складом білки поділяють на протеїни — прості білки, що складаються із залишків молекул амінокислот, і протеїди — складні білки, що складаються із залишків молекул амінокислот і різних небілкових речовин, зокрема йонів металічних елементів.
Хімічні властивості білків
1. Денатурація білків. Під дією різних чинників білки можуть розкладатися, втрачаючи свою специфічну просторову будову. Руйнування просторової структури білка зі збереженням його первинної структури називають денатурацією. Вона відбувається під час нагрівання, зміни кислотності середовища, дії випромінювання або розчинів солей важких металічних елементів та органічних розчинників. Прикладами денатурації є згортання яєчних білків під час варіння яєць або ущільнення білків молока під час скисання.
2. Гідроліз білків. Інша хімічна властивість білків — здатність до гідролізу в кислому або лужному середовищі. Під час гідролізу розриваються пептидні зв’язки і відбувається розщеплення поліпептид-ного ланцюга. Повний гідроліз до окремих амінокислот відбувається під час тривалого нагрівання білків з концентрованою хлоридною кислотою:
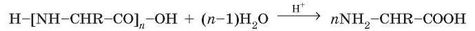
Після потрапляння білкових речовин у шлунок під дією хлорид-ної кислоти і ферменту пепсину відбувається їх гідроліз. Організм людини засвоює білкові речовини тільки у вигляді суміші амінокислот.

3. Кольорові реакції білків. Для виявлення білків або окремих амінокислот у їхньому складі використовують спеціальні якісні реакції, які називають кольоровими реакціями білків.
Так, у разі дії на слаболужний розчин білка розчину купрум(П) сульфату розчин набуває фіолетово-синього забарвлення, що зумовлене зв’язуванням йонів Купруму Cu2+ поліпептидами (мал. 31.1). Цю реакцію називають біуретовою, вона є універсальною для всіх білків, оскільки виявляє наявність пептидних зв’язків.
За допомогою ксантопротеїнової реакції можна виявити ароматичні амінокислоти у складі білків, наприклад тирозин, триптофан, фенілаланін тощо. Для проведення цієї реакції на білок або його розчин діють концентрованою нітратною кислотою. За наявності залишків ароматичних амінокислот білок забарвлюється у жовтий колір (мал. 31.2, а). Після додавання в реакційну суміш розчину амоніаку колір білка поглиблюється і стає жовтогарячим (мал. 31.2, б).
Біологічне значення білків
Білки у живих організмах виконують найрізноманітніші функції, що ви вивчали на уроках біології. Згадаймо найважливіші з них.
Усі без винятку хімічні реакції в організмі відбуваються за наявності спеціальних каталізаторів — ферментів (або ензимів), що являють собою білкові молекули. Вони прискорюють реакції в мільйони разів, причому кожну реакцію каталізує певний фермент.
Деякі білки виконують транспортну функцію — переносять молекули або йони в місця синтезу або накопичення речовин. Наприклад, білок гемоглобін у складі еритроцитів переносить кисень до тканин і вуглекислий газ від них, а білок міоглобін запасає кисень у м’язах.
Білки — це будівельний матеріал клітин, із них побудовані тканини організму.
Білки-рецептори сприймають і передають сигнали, що надходять від сусідніх клітин або з навколишнього середовища. Наприклад, дію світла на сітківку ока сприймає білок родопсин.
Білки життєво необхідні будь-якому організму і тому є найважливішою складовою частиною харчових продуктів. У процесі травлення вони гідролізуються до амінокислот, що є сировиною для синтезу інших білків, необхідних організму.
ЛАБОРАТОРНІ ДОСЛІДИ № 3 ТА 4
Кольорові реакції білків
Обладнання: штатив із пробірками, пальник, пробіркотримач. Реактиви: яєчний білок, луг, купрум(ІІ) сульфат, нітратна кислота, амоніак.
Правила безпеки:
• для виконання дослідів використовуйте невеликі кількості реактивів;
• остерігайтеся потрапляння реактивів на шкіру, в очі, на одяг; у разі потрапляння їдкої речовини змийте її великою кількістю води;
• під час нагрівання не торкайтеся руками гарячих предметів. Лабораторний дослід 3. Біуретова реакція
У пробірку налийте розчин білка об’ємом 1-2 мл і додайте декілька крапель розчину лугу.
У пробірку прилийте трохи розчину купрум(ІІ) сульфату. Як змінюється забарвлення? Про що це свідчить?
Лабораторний дослід 4. Ксантопротеїнова реакція
У пробірку налийте розчин білка об’ємом 2-3 мл і додайте 3-5 крапель нітратної кислоти. Що відбувається?
Уміст пробірки нагрійте в полум’ї пальника. Що відбувається? У пробірку додайте 2-3 мл розчину амоніаку. Що відбувається? Зробіть висновок. Про що свідчать ваші спостереження?
Ключова ідея
Білки — природні полімери, мономерами яких є амінокислоти. Із протеї-
ногенних амінокислот побудовані безліч різних молекул білків, які в живих
організмах виконують різноманітні функції.
Контрольні запитання
488. Які сполуки є білками?
489. За яким параметром білки відносять до полімерів?
490. За яких умов відбувається денатурація та гідроліз білків?
491. Схарактеризуйте біологічну роль білків.
492. Чим відрізняється елементний склад білків від елементного складу вуглеводів та жирів?
493. Які реакції називають кольоровими та для чого їх застосовують?
Завдання для засвоєння матеріалу
Комплексні завдання
494. Під час гідролізу трипептиду масою 46,2 г з натрій гідроксидом утворилася сіль тільки однієї насиченої амінокислоти масою 66,6 г. Визначте цю амінокислоту.
495. Визначте, якою може бути відносна молекулярна маса білка, в якому масова частка Сульфуру становить 0,4 %. Під час обчислень прийміть до уваги, що в молекулі білка щонайменше два залишки молекул амінокислот, у яких по одному атому Сульфуру в молекулі.
Завдання з розвитку критичного мислення
496. У першій пробірці міститься розчин білка, а в другій — гліцеролу. За допомогою яких реакцій можна розрізнити вміст обох пробірок?
497. Як ви вважаєте, чи можна на тривалий час замінити білкову їжу на їжу, що складається тільки з жирів та вуглеводів? Які зміни відбуватимуться в організмі людини за такої дієти?
498. Проаналізуйте наведену діаграму та дайте відповіді на запитання.
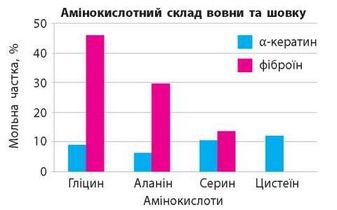
— Яку характеристику двох білків порівнюють на цій діаграмі?
— На діаграмі порівнюють два білки: а-кератин у вовні та фіброїн павутинного шовку. Яким кольором позначено дані про білок, що міститься у вовні?
— Залишків якої амінокислоти найбільше міститься в павутинному фіброїні?
— Яка мольна частка аланіну в а-кератині та фіброїні?
— Визначте мольну частку всіх інших амінокислот, не позначених на діаграмі, для обох білків.
— Павутинний фіброїн набагато міцніший матеріал за а-кератин у вовні. Якби ви були технологом текстильної компанії і перед вами постала задача виготовити якомога міцнішу тканину, то які амінокислоти ви б використали для створення поліпептидного волокна?
Міні-проекти
499. У кабінеті хімії разом з учителем виконайте експериментальний проект. Під час роботи дотримуйтеся правил безпеки.
Дослід 1. Обережно розбийте сире яйце так, щоб не ушкодити жовток. Відокремте невелику частину білка і помістіть її у дві пробірки. Якщо пробірку з білком нагріти на вогні, то слизувата маса стане білою й твердою, як це відбувається під час готування яєчні. Відбувається денатурація білка. На металевому дроті спаліть невеликий шматочок цього білка й понюхайте його. Утворюється характерний запах, що нагадує запах паленого рога, за яким завжди можна впізнати білок. Дослід 2. Уміст другої пробірки обережно змішайте з водою, при цьому білок частково розчиняється. Енергійно струсіть уміст пробірки і спостерігайте утворення тягучої в'язкої маси — у разі механічного впливу білок також піддається денатурації. До тієї ж пробірки додайте розчин солі важкого металічного елемента, наприклад мідного купоросу, і спостерігайте денатурацію під дією йонів металічних елементів. Дослід 3. Якщо потримати над вогнем пташине перо або волосся, відчуєте знайомий запах паленого рога. Це свідчить про те, що перо й волосся містять білок.
Перевірте свої знання за темою «Нітрогеновмісні органічні сполуки», виконавши тестові завдання на сайті.
Це матеріал з підручника Хімія 10 клас Григорович
Наступна сторінка: Високомолекулярні сполуки