Попередня сторінка: Саморегуляція біологічних систем
Наступна сторінка: Саморегуляція на клітинному рівні
Поміркуйте
Для чого клітина регулює швидкість роботи ферментів?
Згадайте
• Ферменти
• Метаболічні шляхи
• Каталітичний центр ферменту
• Алостерична регуляція
Загальні шляхи регуляції активності ферментів
Регуляція активності ферментів спрямовує всі клітинні процеси. Ферменти здатні реагувати на внутрішній стан клітини й на зовнішні фактори, що впливають на неї. Така чутливість ферментів дає змогу відреагувати на зміни навколишнього середовища, пристосувати клітину до нових умов, дати відповідь на гормональні сигнали.
Рівень активності ферментів регулюється двома шляхами: контролем кількості ферменту й контролем його активності. Кількість ферменту визначається співвідношенням швидкостей його синтезу й розпаду. Кількість ферменту змінюється залежно від інтенсивності його синтезу. Цей процес регулюється на етапах експресії гена цього ферменту (докладніше див. § 22).
Контроль активності ферменту здійснюється шляхом взаємодії з певними речовинами, що змінюють конформацію активного центру. Як ви знаєте, ферменти за своєю природою є білками. І їхня чутливість до субстрату залежить від просторової конфігурації.
Доступність субстрату
Одним із простих способів регуляції активності ферментів є зміна концентрації субстратів реакції. Як ви знаєте, швидкість, із якою речовини реагують між собою, залежить від їхньої концентрації. Чим більше
молекул субстрату є в наявності, тим швидшим стає процес. При насиченні всіх молекул ферменту субстратом швидкість реакції стає максимальною. Наприклад, для циклу трикарбонових кислот таким субстратом виступає оксалоацетат. Наявність оксалоацета-ту «підштовхує» реакції циклу.
Алостерична регуляція
Алостерична регуляція ферментної активності базується на зміні третинної структури молекул ферменту. Ця зміна відбувається внаслідок приєднання до ферменту молекули іншої речовини.
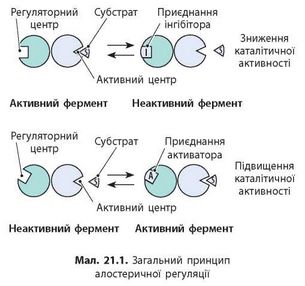
Алостеричні ферменти мають два активні центри: каталітичний і алостеричний. До алостеричного центру приєднується молекула речовини-ефектора. Це змінює конформацію білка й, відповідно, його ферментну активність (мал. 21.1).
Алостерична регуляція може бути як позитивною, так і негативною. Негативним регулятором може бути кінцевий метаболіт біохімічного процесу або продукт цієї реакції, тобто діє механізм негативного зворотного зв’язку (мал. 20.1). Позитивним регулятором може бути субстрат реакції; у такому випадку діє механізм позитивного зворотного зв’язку.
Хімічна регуляція
На активність ферментів можна вплинути шляхом їхньої хімічної модифікації. Хімічна модифікація здійснюється приєднанням до амінокислот білка певних груп: фосфатної групи, залишку жирної кислоти, вуглеводних компонентів. Приєднання додаткових угруповань суттєво впливає на структуру ферменту, а отже, і на його ферментативну активність.
Найбільш поширений спосіб змінити властивості білків — це фосфорилюван-ня й дефосфорилювання (приєднання або від’єднання залишку фосфорної кислоти). Наприклад, під час фосфорилювання білків клітинного цитоскелета змінюється сила його взаємодії з мембраною й форма клітин. Фос-форилювання певних білків активує скорочення м’язів.
Обмежений протеоліз
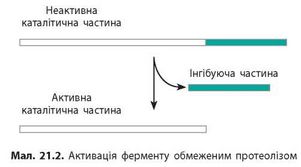
Обмежений (частковий) протеоліз передбачає, що синтез деяких ферментів здійснюється у вигляді більшого попередника — проферменту. Фермент активується шляхом відщеплення від нього одного або кількох пептидних фрагментів. Тоді в частині молекули, що залишилася, відбувається конфор-маційна перебудова й формується активний центр (мал. 21.2). Фермент стає активним.
Прикладом є активація протеолітичних ферментів шлунково-кишкового тракту (трипсиногену, пепсиногену), факторів системи зсідання крові (фібриногену), лізосомаль-них ферментів, пептидних гормонів (інсуліну). Наприклад, неактивний трипсиноген, синтезований у підшлунковій залозі, надходить у кишечник, де відбувається його обмежений протеоліз. У результаті утворюється активний трипсин.
Такий механізм захищає організм від ушкоджень (наприклад, щоб слизова підшлункової залози не зруйнувалася під дією трипсину) або зберігає білок до моменту,
коли знадобиться його активність (під час згортання крові).
Метаболічні ланцюги
Зазвичай ферментативні реакції в клітині об’єднані в метаболічні ланцюги або цикли.
У кожного метаболічного ланцюга є ключовий фермент, який визначає швидкість усього ланцюжка реакцій. Як правило, ключові ферменти є першими в ланцюжку. Найчастіше це алостеричні ферменти. Вони інгібуються кінцевими продуктами або активуються субстратами (мал. 20.1). У такий спосіб регулюється швидкість усього метаболічного шляху.
Також функціонування клітини забезпечується просторовою регуляцією метаболічних шляхів. Цей тип регуляції пов’язаний із локалізацією певних ферментів у різних органелах: у ядрі містяться ферменти синтезу ДНК і РНК, у цитоплазмі — ферменти гліколізу, у мітохондріях — ферменти циклу трикарбонових кислот. Найвищий рівень просторової організації спостерігається, коли ферментні комплекси пов’язані з мембранами. У такому разі речовини, що перетворюються, послідовно пересуваються вздовж ланцюга ферментів. Приклади таких комплексів — АТФази і переносники електронів у мембранах хлоропластів і мітохондрій. Чітка просторова локалізація ферментів у клітині забезпечує їх узгоджену діяльність.
Ключова ідея
Регуляція активності ферментів спрямовує всі клітинні процеси. Рівень ферментної активності регулюється двома шляхами: контролем кількості ферменту й контролем його активності.
Запитання та завдання
1. Алостеричні ферменти найчастіше мають четвертинну структуру: складаються з декількох суб-одиниць. Чому? 2. Як ви вважаєте, які з розглянутих способів регуляції активності ферментів є оборотними, а які — необоротними?
Це матеріал з підручника Біологія і екологія 11 клас Задорожний (профільний рівень)
Наступна сторінка: Саморегуляція на клітинному рівні