Попередня сторінка: Металічний зв'язок
Наступна сторінка: Залежність фізичних властивостей реч�...
За внутрішньою будовою і фізичними властивостями розрізняють два стани твердих речовин: аморфний і кристалічний.

Кристалічні речовини:
• структурні одиниці розташовані в чіткому порядку — утворюють кристалічні ґратки;
• мають певну температуру плавлення;
• утворюють кристали певної форми;
• у разі руйнування кристалічної речовини кристали розпадаються на окремі шматочки, кожен із яких зберігає хоча б частково форму початкового кристалу;
• приклади речовин: природні мінерали, кухонна сіль, цукор.
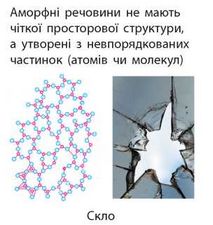
Аморфні речовини:
• не мають чіткої просторової структури — структурні одиниці розташовані невпорядковано;
• плавляться в певному діапазоні температур;
• за нагрівання спочатку розм’якшуються;
• у разі руйнування утворюються уламки неправильної форми, зазвичай із нерівною поверхнею країв сколу;
• приклади речовин: скло, смоли, бурштин, застиглі лаки, клеї, каучук.

Аморфні речовини за внутрішньою будовою нагадують рідини, тільки не можуть текти. Під час нагрівання вони поступово розм’якшуються і нарешті стають рідкими. Аморфним речовинам, як і рідинам, можна надати будь-якої форми.
За певних умов речовина може з кристалічної перетворюватися на аморфну, і навпаки. Звичайне скло — аморфна речовина, але із часом силіцій(ГУ) оксид у його складі набуває кристалічної форми. Через це старі склянки під час наливання в них окропу лопаються набагато частіше, ніж нові. Цукор — кристалічна речовина. Але якщо його розплавити та швидко охолодити, то він застигає в аморфному стані. З такого цукру можна виготовляти льодяники, карамельки тощо (мал. 9.1).
Штучні монокристали
Від 1955 року в Україні працює Науково-технологічний комплекс «Інститут монокристалів» НАН України (м. Харків). Це потужний науковий і виробничий комплекс, де проводять дослідження з перспективних сучасних напрямків фізики та хімії. Внесок українських учених у сучасну науку визнаний багатьма світовими науковцями. Але, крім наукової роботи, значну увагу в цьому інституті приділяють виробництву. Головний напрямок виробничої діяльності — синтез штучних правильних індивідуальних незрощених кристалів. Багато з них виробляють для внутрішнього використання, але великі обсяги кристалів експортуються. Монокристали дуже міцні і мають широке застосування. Із сапфірових монокристалів (алюміній оксид) виробляють надійні захисні пластини для отворів оптичних приладів. Такі пластини Інститут монокристалів постачає для української армії: ними оснащують оглядові віконця бронетехніки. Крім сапфірів, Інститут монокристалів виробляє кристали на основі оксидів Молібдену, Плюмбуму, Церію, Германію тощо, кристали з калій дигідрогенортофосфату, кадмій вольфрамату та інших речовин. Такі кристали використовують як елементи нелінійних оптичних лазерів, як сцинтиляційні матеріали для уловлювання та детектування гамма-і рентгенівського випромінювання.
Корисні дефекти
Зазвичай, коли йдеться про дефекти в будь-чому, то мають на увазі щось негативне і шкідливе. Але трапляються випадки, коли через появу дефектів виникають нові, корисні властивості. Найкращий приклад — поява дефектів у спадковій інформації, що призвело до еволюції життя, хоча існують і менш значущі випадки.

звичайна кам'яна сіль має бути білою, хоча в продажу є кухонна сіль різних кольорів: від рожевої до чорної. Такі кольори сіль має через додавання певних домішок. Проте в природі трапляються мінерали галіту — досить чистого натрій хлориду — синього кольору.
Така сіль не містить забарвлених домішок, а колір виникає виключно внаслідок дефектів у кристалічних ґратках натрій хлориду. Під час утворення кристалу, особливо якщо ріст кристалу відбувається швидко, можуть виникати «збої» у побудові правильних ґраток. Або такі дефекти можуть виникати внаслідок дії на кристали гамма-випромінюванням, що в невеликій інтенсивності завжди існує в природі. Дослідження синього натрій хлориду виявили, що в певних місцях кристалічних ґраток замість хлорид-іонів містяться вільні електрони, наявність яких і зумовлює забарвлення. Певна річ, що після розчинення такої солі у воді вільні електрони зникають, і утворюється звичайний безбарвний солоний розчин. Дефекти у кристалах можна створювати штучно з певною метою. Так, робота всіх сучасних електронних пристроїв ґрунтується на напівпровідникових властивостях силіцію, з якого виготовляють усі мікрочіпи для електроніки. Не дарма місце в Каліфорнії, де розташовані найбільші світові корпорації з новітніх технологій, називають Силіконовою долиною. Але напівпровідникові властивості силіцію можна значно покращити шляхом додавання до нього домішок (у залишкових кількостях), які утворюють «корисні» дефекти в кристалічних ґратках силіцію. Найчастіше під час вирощування кристалів силіцію додають невеликі кількості бору чи арсену.
Ключова ідея
Для аморфних речовин порядок у розташуванні частинок характерний тільки на відстані однієї-двох структурних частинок. У кристалічних речовинах порядок розташування частинок характерний для всього об'єму монокристала.
Контрольні запитання
117. Назвіть спільні властивості всіх твердих речовин.
118. Які речовини називають кристалічними, а які — аморфними?
119. Назвіть ознаки кристалічних та аморфних речовин. Наведіть приклади таких речовин.
Завдання для засвоєння матеріалу
120. Схарактеризуйте основні відмінності у фізичних властивостях кристалічних та аморфних речовин.
121. Визначте спільні та відмінні риси у рідин та твердих аморфних речовин.
122. Чи є аморфними речовинами віск, парафін, сухий лід, поліетилен, скло, кухонна сіль, тверде мило? Відповідь обґрунтуйте.
Завдання з розвитку критичного мислення
123. Як ви вважаєте, чому аморфні речовини не мають чіткої температури плавлення? Чому кристалічні речовини не розм'якшуються перед плавленням?
124. Як ви розумієте твердження: «Кристалічним речовинам не можна надати будь-якої форми»?
125. Як ви вважаєте, чому за швидкого охолодження розплавленого цукру він застигає в аморфному стані, а не в кристалічному?
126. Аморфний стан характерний для бурштину, бітумів, асфальтів, вищих ал-канів тощо. Які особливості молекул цих речовин зумовлюють їх існування в аморфному стані?
127. Скористайтеся додатковими джерелами інформації та проаналізуйте, як узгоджується ключова ідея цього параграфа з твердженням: «Для кристалічних речовин характерний дальній порядок розташування частинок, а для аморфних — ближній».
Це матеріал з підручника Хімія 11 клас Григорович
Наступна сторінка: Залежність фізичних властивостей реч�...