Попередня сторінка: 14. A nemfémes elemek
Наступна сторінка: 16. A nemfémek fizikai tulajdonságai. Az adszorpció
E téma tananyaga segít nektek:
felidézni a legfontosabb nemfémekről szerzett ismereteket;
ismereteket szerezni az allotrópia jelenségéről; megérteni, hogy egyfajta kémiai elem alkotta egyszerű anyagok hogyan különbözhetnek egymástól; ismereteket szerezni a nemfémek mint egyszerű anyagok természetben való elterjedéséről.
A nemfémes elemek egyszerű anyagokat képeznek, amelyek neve nemfémek (26. ábra). Ezek általában eltérnek a fémektől a megjelenés, a fizikai tulajdonságok és gyakran a normál körülmények közötti halmazállapotok szerint. Ezek a különbségek a nemfémes szerkezetek sajátosságaiból adódnak.
A nemfémek szerkezete. A nemfémek egy része atomszerkezettel rendelkezik. A nemesgázok - hélium, neon, argon, kripton, xenon és radon - nemesgázatomokból állnak. A grafitban, gyémántban, szilíciumban, borban, vörösfoszforban szintén atomok kapcsolódnak egymáshoz.

26. ábra
Nemfémek
A többi nemfém molekuláris szerkezetű anyag. Vannak olyan nemfémek, melyek molekulái kétatomosak, (nevezzétek meg ezeket az anyagokat.), de akad többatomos molekula is: O3 - ózon, P4 - fehérfoszfor, S8 - kénmolekula.
Az elemmolekulák atomjai között kovalens apoláris kötés található: egyszerű, kettős vagy hármas.
Az allotrópia. Néhány nemfémes elem esetében két vagy több egyszerű anyag ismert.
Az elemeknek azt a tulaj donságát, hogy több egyszerű anyagot alkothatnak, allotrópiának1 nevezzük.
Ugyanazon elem egyszerű anyagai (allotrop módosulatai) különbözhetnek egymástól szerkezetükben, a molekulát alkotó atomok számában, előállítási módjában. Mindez befolyásolja az anyagok fizikai tulajdonságait, és bizonyos esetekben a kémiai aktivitását is.
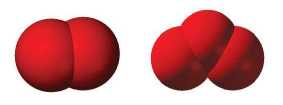
Az oxigén mint egyszerű anyag. Az oxigénatom két egyszerű anyagot alkothat: O2 -oxigéngáz (erről már tanultunk), és O3 - ózon (27. ábra). Az ózon jellegzetes szagú, mérgező gáz. Olvadás- és forráspontja magasabb, mint az oxigéngázé. Az ózonnak az oxigénnél nagyobb a kémiai aktivitása.
27. ábra
Az O2 és az O3
nagyszabású
modellje
A szén mint egyszerű anyag. A mindennapi szóhasználatban a szén szó a már tanult ásványi szenet jelenti. A természetes elemi szén két kristályos (atomszerkezetű) módosulata a gyémánt és a graűt régóta ismert anyagok; a molekuláris szerkezetű fullerén a múlt század felfedezése (28. ábra). Az ábrán látható fullerén-molekula 60 atomból áll.
1 Az allotrópia elnevezés a görög allosz - jelentése más, és tropos -jelentése mód, helyzet szóból származik.
2 Előállítottak olyan egyszerű anyagokat is, melyeknek molekulái 70 vagy több szénatomot tartalmaznak.
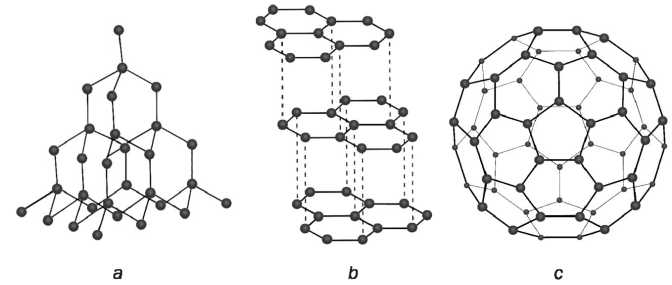
28. ábra
Ászén módosulatainak szerkezete: a - a gyémánt-kristály részlete; b - a grafit kristály-rácsának részlete; c - a fullerén-mole-kula modellje
A gyémánt tiszta állapotban színtelen, átlátszó, nagy fénytörő képességű anyag. Az elektromos áramot nem vezeti. A legkeményebb természetes ásvány. A gyémántban minden egyes szénatom négy kovalens apoláris kötéssel kapcsolódik másik négy szénatomhoz (28. a ábra).
A grafit sötétszürke, átlátszatlan, fémes fényű anyag. A hőt és az elektromosságot jól vezeti. Rácsa réteges szerkezetű. A szénatomok úgy helyezkednek el benne, mintha több síkban méhsejtszerüen egymás mellett, a benzolhoz hasonló hatszög alakú széngyűrűk lennének. Egy szénatom három másik szénatommal kapcsolódik egyszeres (o-) kovalens kötéssel. A szénatomok negyedik vegyértékelektronja nem vesz részt kémiai kötések kialakításában. Ezek az elektronok delokalizáltak (hasonlóan a benzol p-elektronrendszeréhez). Ennek köszönhető az, hogy a grafit jól vezeti az elektromos áramot, és az is, hogy a grafit fekete színű. Az ilyen méhsejt-szerű rétegek egymással párhuzamosan, kicsit távolabb, lazább kötéssel helyezkednek el. Mivel két réteg között nagyobb a molekulatávolság, gyengébb a kötés, a rétegek könnyen szétválnak, így a grafit nyomot hagy a papíron.
A C60 fullerénmolekula 20 hatszöghői és 12 ötszöghői készült futball-labdára hasonlít (28. c ábra).
Néha az ásványi szenet is a szénatom módosulataihoz számítják, bár ebben az anyagban a szénatomok mellett más atomok is vannak. Tiszta, szinte
teljes egészében szénatomokból álló Einyag előállítható fa hevítésével oxigénmentes környezetben. A fa fokozatossm elszenesedik és a berendezésből vízgőz, VEdamint kellemetlen szagú gáz hEÚmazálla-potú anyagok távoznak. A pirolízis után keletkező fekete anyag koromszerű elemi szén. Ezt eiz anyagot amorf szénnek is nevezik, mert a szénatomok elhelyezkedése kaotikus benne.
A kén mint egyszerű anyag. Ez elz elem két nagyon hasonló kristályos szerkezetű egyszerű Emyagot képez — rombos és monoklin ként. Ezek UgysmEizokat az S8-molekulákat tartalmazzák, de az Emyagok kristályaibEm való elrendezésük eltérő (29. ábra).
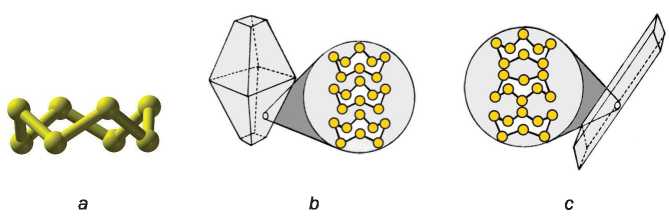
29. ábra
Az S8 molekula gömbpálcika modellje (a).
A rombos (b) és a monoklin (c) kénkrlstály szerkezete
На a ként megolvasztják, szinte forrásig, majd az olvadt ként hideg vízbe öntik, az nyúlós, gumiszerű anyaggá dermed. Ez az amorf kén (30. ábra), amely 2-4-atomos láncmolekulákból áll. Idővel visszaáll benne az eredeti kristályos szerkezet: S8 gyűrűs szerkezetű molekulák képződnek, és az amorf kén fokozatosan szilárd és törékeny rombos kénné alakul.

30. ábra
Amorf kén előállítása
A foszfor mint egyszerű anyag. A foszfor atomjai többféle egyszerű Emyagot képezhetnek. A fehérfoszfor és a vörösfoszfor a foszfor két Eillotrop módosulata. A fehérfoszfor P4-molekulákból áll, a vörösfoszfor pedig egymással kovalens kötéssel összekapcsolt atomokból (31. ábra).
A fehérfoszfor, a vöröstől eltérően, fokhagyma illatú, nagyon mérgező anyag. Kémiailag aktívabb, mint a vörösfoszfor. A fehérfoszfor levegő jelenlétében már 50 °C-nál sötétben jól látható fénykibocsátás közben oxidálódik (ezért csak víz alatt tárolható).

31. ábra
A foszfor
allotrop
módosulatai
A nemfémek elterjedtsége a természetben. Tudjuk, hogy a levegő fő összetevői a nitrogén és az oxigén, de kis mennyiségű nemesgázokat is tartalmaz (nagyobbrészt argont). A légkör felső rétegében a legkisebb tömegű gázok találhatóak: a hidrogén és a hélium. A légkörben nagyon kis mennyiségű ózon is van, amely az úgynevezett ózonrétegben, 20-25 km magasságban koncentrálódik. Ez a finom eloszlású ózonréteg kozmikus sugárzás vagy elektromos kisülés hatására (villámlás esetén) képződik oxigénből:
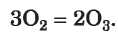
Mivel az ózonmolekulák instabilak, így a fordított reakció is végbemegy. Az ózon elnyeli az élő szervezetekre káros ultraibolya sugarakat és ismét oxigénmolekula keletkezik.
A természetben, a magas légrétegekben az ózon keletkezése és elbomlása egyidőben játszódik le. Ha idegen anyagok nem szennyeznék ezeket a rétegeket, az ózonnak a kialakult mennyisége állandó lenne. Az emberi tevékenység során sok olyan anyag kerül a levegőbe, amely az ózon bomlását gyorsítja. Jelenleg az ózonréteg megőrzése érdekében különböző intézkedéseket hoznak.
A földkéregben három nemfém található tiszta állapotban: a kén, a grafit és a gyémánt. Ukrajnában kén- (Lviv, Ivano-Frankivszk és Temopil megyében) és grafitlelőhelyek (a Kirovogradi és Zaporizsjai megyében) találhatók.
Szerintetek miért nincsenek a természetben szabad állapotban a halogének: a fluor, a klór, a bróm és a jód?
ÖSSZEFOGLALÁS
A nemfémek a nemfémes elemek egyszerű anyagai. Néhány nemfémes elem több egyszerű anyagot alkot, melyek szerkezete és fizikai tulajdonságai különböznek egymástól. Az ilyen jelenséget allotrópiának nevezik.
A nemfémek többsége molekuláris szerkezetű, néhány azonban atomokból épül fel.
A nemfémek előfordulása a természetben gyakori. A levegő fő összetevői a nitrogén és az oxigén, a földkéregben található a kén, a grafit, a gyémánt.
Az ózon a légkörben úgynevezett ózonréteget alkot, ami elnyeli az ibolyántúli sugárzás egy részét és ezáltal védi a bioszférát.
107. Melyik kijelentésben beszélünk a halogénekről mint kémiai elemről, és melyikben mint egyszerű anyagról:
a) a halogének színes anyagok;
b) a halogének a halogenidek elnevezésű vegyületek összetételében találhatók;
c) a halogének aktív nemfémek;
d) a halogének elektronegativitása meglehetősen magas.
108. Miben különböznek egymástól a) az oxigén, b) a szén allotrop módosulatai?
109. Jellemezzétek az S2-molekulában található kötést (ilyen molekulából áll a kéngőz).
HO. A gyakorlatban milyen tulajdonságát alkalmazzák a grafitnak? Magyarázzátok el ezt a tulajdonságát szerkezete alapján.
111. Mivel magyarázható, hogy a fehérfoszfor nagyobb aktivitást mutat, mint a vörösfoszfor? Várható-e a kén allotrop módosulatainál ilyen különbözőség? Indokoljátok meg a feleletet.
112. Milyen anyagmennyiséggel rendelkezik a) 0,48 g ózon; b) 4,48 1 argon (n.k.k.) (Szóbelileg).
113. Az oxigénnel alkotott keverékben az ózon tömegszázaléka 7,2%. Számítsátok ki az ózon térfogatszázalékát ebben a keverékben.
Ez a tankönyv anyaga Kémia a 11. osztály számára Pavlo Popéi
Наступна сторінка: 16. A nemfémek fizikai tulajdonságai. Az adszorpció