Попередня сторінка: 7. A hidrogénkötés. A fémes kötés
Наступна сторінка: 9. Egyirányú és megfordítható kémiai reakciók
E téma tananyaga segít nektek:
ismereteket szerezni a szilárd anyagok csoportosításáról;
megkülönböztetni a kristályos és az amorf anyagokat tulajdonságaik alapján.
A konyhasó, a cukor, a liszt, a keményítő mind fontos élelmiszer. Naponta találkozunk velük és tudjuk, hogy a konyhasó és a cukor kristályos, a lisztet és a keményítőt felépítő részecskék nem hasonlítanak kristályokra. Ezt megerősíti az utóbbi két anyag mikroszkóppal való vizsgálata is.
A szilárd anyagok az őket felépítő részecskék elrendeződése alapján két csoportba sorolhatók: kristályos és amorf1 anyagok.
A kristályos anyagok. A 8. osztályban az ionos vegyületeknél már tanultatok arról, hogy ezek kristályokat (11. ábra) alkotnak. A kristályos anyagok szilárd anyagok, melyeket síklapok határolnak és a részecskék bennük szabályos rendben helyezkednek el, kristályrácsot alkotnak.

11. ábra
Ásványi anyagok mintái
A konyhasó kristályai kockaformájúak, a cukorkristályok összetettebb alakzatúak. A kristályt alkotó legkisebb részecske a konyhasó esetében a Na+ és a CT -ionok, a cukor esetében a
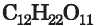
-molekulák,
melyek elrendeződése a tér minden irányában szabályos és sokszorosan ismétlődő.
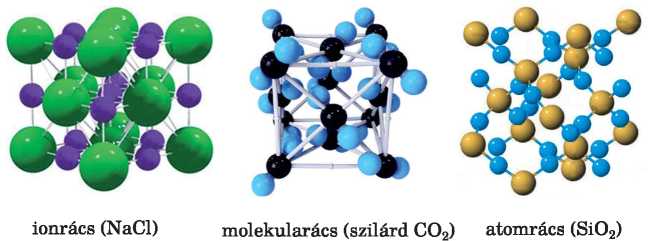
A kristály szerkezetének modellje a kristályrács. A kristályokban a részecskéknek szabályos elhelyezkedése egy váltakozó csomópontokkal rendelkező rács szerkezetére emlékeztet, innen ered a kristályrács elnevezés is. A kristály rácspontjaiban található anyagi részecskék és a közöttük működő erők típusa szerint négyféle rácstípust különböztetünk meg: ionrács, molekularács, atomrács és fémrács (12. ábra).
12. ábra
Kristályrácsok
(gömb-pálcika
modellek)
1 Az elnevezés a görög amorphos — alaktalan szóból ered.
Milyen színű golyók felelnek meg a szén-, a szilícium- és az oxigénatomnak a 12. ábrán látható kristályrácsokban?
Érdekes
tudnivaló
A kristályos anyag szerkezetét a röntgensugár kristály általi visszaverődésével tanulmányozzák.
Alacsony hőmérsékleten vagy közönséges körülmények között a legtöbb egyszerű anyag, szervetlen vegyület és a szerves anyagok közül a kismole-kulájúak kristályos szerkezettel rendelkeznek.
Az amorf anyagok. Vannak anyagok, melyekben az azokat felépítő részecskék - atomok, molekulák elhelyezkedése rendezetlen, vagy csak kis körzetekben rendezett. Ezek az amorf anyagok (13. ábra). Ez a szerkezet a cseppfolyós anyagokra jellemző.

13. ábra
A kristályos anyag (a) és az amorf anyag (b) szerkezete
Az amorf anyagokban (és a folyadékokban) a részecskék elhelyezkedése csak kis körzetekben rendezett, míg a nagyobb távolságra elhelyezkedők gyengébben kötődnek egymáshoz, így nincs bennük rendezettség. így például a hidrogénkötés szabályozza a poliszacharidok és a fehérjék szomszédos molekuláit; a vizes oldatok intermo-lekuláris kölcsönhatásáról már szereztetek ismereteket.
Az amorf anyagokhoz tartoznak a zsírsavak, a poliszacharidok, a zsírok, a fehérjék, az óriásmolekulájú anyagok. Szervetlen amorf anyag az üveg, bár lehet készíteni belőle olyan tárgyat, melyet külső megjelenés alapján nehezen különböztetünk meg a kristálytól, viszont ütés hatására meghatározhatatlan alakú darabokra törik szét. Ez történik a borostyán esetében is.
Fizikai tulajdonságok. A kristályos és az amorf anyagok egyes fizikai tulajdonságaikban is különböznek egymástól. A kristályos anyagok,
melyek hőmérséklet hatására nem bomlanak fel meghatározott hőmérsékleti ponton, olvadásponton olvadnak meg; az amorf anyagoknak nincs éles olvadáspontjuk, hanem egy adott hőmérsékleti tartományban olvadnak meg. Például az üveg hőmérséklet hatására fokozatosan meglágyul (eközben folytatódik a melegítés), utána egy viszkózus folyadékká válik.
A szénatomot kettős kötéssel kapcsoljuk össze. Az amorf anyagok keménysége, optikai tulajdonságai - a kristályos anyagoktól eltérően - nem attól függnek, hogy a külső erő milyen irányból hat, vagy merről jön a fénysugár; ezek hatása minden irányban azonos.
Érdekes
tudnivaló
Aszilícium-oxid megtalálható kristályos formában (pl. a kvarc) és amorf formában is (kvarcüveg).
ÖSSZEFOGLALÁS
A szilárd anyagok lehetnek kristályos és amorf szerkezetűek. A kristályos anyagok szilárd anyagok, melyeket síklapok határolnak és a részecskék szabályos rendben helyezkednek el bennük. A kristály szerkezetének modellje a kristályrács. A kristályt alkotó részecskék elhelyezkedése rendezett, az amorf anyagban rendezetlen. A kristályos anyag olvadáspontja meghatározott, az amorf anyag egy adott hőmérsékleti tartományban olvad meg.
64. Milyen halmazállapotokat ismerünk? Hozzatok fel 2-3 példát olyan anyagokra, melyek mindhárom halmazállapotban megtalálhatók. Szükség esetén a megfelelő információra keressetek rá az interneten.
65. A nátrium-klorid kristályrácsának ábrázolását használva (12. ábra) határozzátok meg, mennyi Cl- -ion veszi körül mindegyik Na+-iont, és mennyi Na+-ion veszi körül mindegyik Qr -iont a só kristályában.
66. A citromsav kristályos anyag. Milyen részecskék - atomok, molekulák vagy ionok - alkotják a kristályrácsát?
67. Milyen típusú kristályráccsal rendelkeznek az alábbi anyagok: bárium-hidroxid, aliunínium-szulfát, grafit, foszfor(V)-oxid (a valós képlete P4O10)?
68. Képzeljétek el, hogy a szilárd zsír nem tartalmaz keverékanyagot, tiszta anyag. Milyen az olvadáspontja: meghatározott vagy egy bizonyos intervallumban olvad? A feleletet indokoljátok.
Ez a tankönyv anyaga Kémia a 11. osztály számára Pavlo Popéi
Наступна сторінка: 9. Egyirányú és megfordítható kémiai reakciók