Попередня сторінка: 32. A kémiai elemek biológiai jelentősége
Наступна сторінка: 34. A kémia és a civilizáció fejlődése
E téma tananyaga segít nektek:
megismételni az egyszerű anyagok és a szervetlen vegyületek kémiai tulajdonságait; bővíteni ismereteiteket a különböző csoportokba tartozó vegyületek közötti átalakítási lehetőségekről.
Már tudjátok, hogy az egy és ugyanazon elem által képződött anyagok között kapcsolatok vannak, és kémiai tulajdonságaikat figyelembe véve egyik a másikba átalakítható. Ezeket a kapcsolatokat származási (genetikai) kapcsolatoknak nevezik. Ebben a paragrafusban az egyszerű anyagok és vegyületeik közötti összefüggést és átalakításaikat vizsgáljuk meg, egyben összegezzük a szervetlen vegyületek osztályozásával és kémiai tulajdonságaival kapcsolatos ismereteket (az összefoglaló táblázatok a Függelékben találhatók).
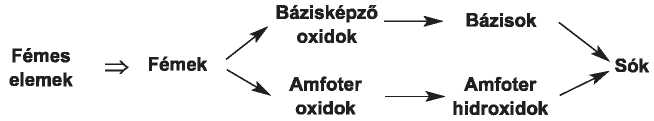
Az anyagok közötti kapcsolat az eredetükkel magyarázható. A fémes elemek egyszerű anyagai a fémek, ezek bázisképző vagy amfoter oxidokat alkotnak1. A bázisképző oxidok a bázisoknak, az amfoter oxidok az amfoter hidroxidoknak felelnek meg (10. vázlat). Az oxidokban, a hidroxidokban, a sók többségében a fémes elemek fém-kationként vannak jelen.
10. vázlat
A fémes elemekből származó anyagok közötti származási kapcsolatok
A nemfémes elemek egyszerű anyagként olyan nemfémek, amelyek savképző oxidokat alkotnak2. Ezekből az oxidokból származnak az oxigéntartalmú savak (11. vázlat). Ezekben a vegyületekben vannak az anionok, amelyek a savalkotó elemet tartalmazzák.
11. vázlat
A nemfémes elemekből származó anyagok közötti származási kapcsolatok

Mindkét vázlat kiegészíthető, illetve egymáshoz kapcsolható. Hiszen azok a sók, melyek biná-

ris vegyületek, fémes, valamint nemfémes elemekből (a periódusos rendszer VI. és VII. csoportjának elemei - kivétel az oxigén) állnak. Ezek az oxigénmentes savak sói, melyek fém-kationt és nemfém-aniont tartalmaznak
A kémiai tulajdonságok alapján kialakuló kapcsolatok. Egyszerű és összetett anyagok részvételével történő kémiai reakciók végbemehetnek oldatokban vagy szilárd halmazállapotú keverékekben, normál körülmények között vagy hőmérséklet hatására, katalizátor jelenlétében vagy nélküle. Egyes reakciókban az elemek oxidációs száma változik, másokban nem, vagyis az anyagok között a reakciók lehetnek változatosak.
Az egyszerű anyagok részvételével végbemenő kémiai átalakulások. A fémek és a nemfémek (egyes kivételtől eltekintve) oxidok keletkezésével reagálnak az oxigénnel:
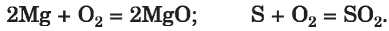
Érdekes
tudnivaló
A nátrium oxigénnel való reakciója eredményeként Na2O2 peroxid keletkezik Na2O keverékkel.
Az alkáli- és alkáli földfémek reakcióba lépnek a vízzel, a fémek többsége savakkal és sókkal. A reakciók lehetősége és lefolyásának sajátosságai a fémnek a fémek aktivitási sorában való elhelyezkedésétől függ. Ezekre a kölcsönhatásokra példa a következő két reakcióegyenlet:

Nevezzétek meg a vas és a sósav, valamint a réz(13)-szulfát között lejátszódó reakciók termékeit.
Az aktívabb nemfémek reagálnak vízzel, lúggal, sókkal:
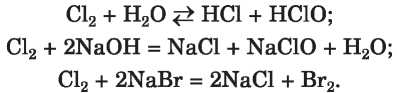
Jegyezzétek meg: az egyszerű anyagok részvételével végbemenő kémiai átalakulások oxidációsredukciós folyamatok.
Az oxidokkal és az oxidok hidrátjaival végbemenő kémiai átalakulások. Az alkáli- és
az alkáli földfémek oxidjai reagálnak vízzel; a reakció terméke lúg (vízben oldódó bázis) vagy vízben kevésbé oldódó bázis. A savképző oxidok vízzel reagálva (kivétel a SiO2) savat alkotnak. Látható, hogy az oxidok és a vízzel való kölcsönhatás termékei hasonló kémiai jelleggel rendelkeznek: bázisos vagy savas:
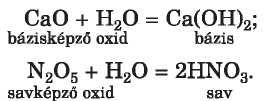
A folyamat visszafelé is igaz. A vízben nem oldódó bázisok hő hatására bázisképző oxidra bomlanak, az oxigéntartalmú savakból savképző oxidok keletkeznek (a szénsav és a kénessav esetében már közönséges körülmények között is végbemegy ez a folyamat). Az amfoter hidroxidok termikus bomlásánál amfoter oxid és víz keletkezik.
Érdekes
tudnivaló
A metafoszfor-sav az egyetlen oxigéntartalmú sav, mely még magas hőmérsékleten sem bomlik fel.
írjátok fel a króm(III)-hidroxid termikus bomlásának reakcióegyenletét.
Számos kémiai átalakulás van különböző jellegű összetett anyagok között. Mindegyik savbázis reakció során megfelelő só keletkezik. Bázisképző oxidok és bázisok savképző oxidok-kal és savakkal lépnek reakcióba. Az amfoter oxidok és a hidroxidok savas és lúgos jellegű anyagokkal is reagálnak:
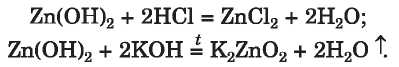
írjátok fel a cink-hidroxid és a kálium-hidroxid vizes oldata között lejátszódó reakció egyenletét.
Jegyezzétek meg: két azonos kémiai jellegű anyag - bázis, amfoter vagy sav - nem lép reakcióba egymással.
A sók részvételével végbemenő kémiai átalakulások. A sók nem mutatnak sem bázisos, sem savas tulajdonságot. A só lúggal való reakciójánál új bázis és só, savval való kölcsön-
hatásánál új sav és só keletkezik; két só közötti kölcsönhatásnál a reakciótermék két másik só:
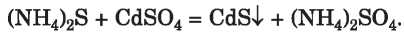
Némely szabályos só vízben való oldódásánál kölcsönhatásba lép az oldószerrel és hidrolízis megy végbe, melynek eredményeként savas vagy bázisos só képződik:
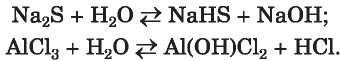
A savanyú sóhoz lúgot vagy a bázisos sóhoz savat adva, újra szabályos sót kapunk:
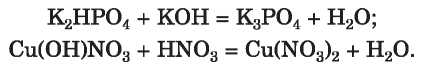
Számos só hőmérséklet hatására felbomlik:
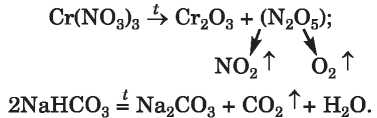
Az anyagok folyamatos átalakításait gyakran megfelelő vázlatokkal szemléltetik, amelyekben fel lehet tüntetve a kiinduló, a köztes és a keletkező anyag; felírhatják a reagensek képleteit, illetve a reakciók feltételeit.

A paragrafusban található tananyag a 13. táblázatban van röviden összefoglalva.
Több olyan átalakítási reakció ismeretes, amikor egy csoportba tartozó anyagot azonos csoportba tartozó más anyaggá alakítanak. Az ilyen reakciók példái:
• oxid átalakítása másik oxiddá
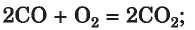
• bázis átalakítása másik bázissá
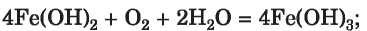
• oxigéntartalmú savból egy másik oxigéntartalmú savat kapunk
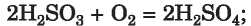
• szabályos sóból egy másik só keletkezik
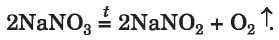
13. táblázat
Kémiai átalakulások
különböző vegyületcsoportba tartozó anyagok részvételével
ÖSSZEFOGLALÁS
Azokat az anyagok közötti kapcsolatokat, amelyek származásukon és kémiai tulajdonságaikon alapulnak, származási (genetikai) kapcsolatoknak nevezik.
A fémes elemekből származnak a fémek, a bázisképző vagy amfoter oxidok, a bázisok vagy az amfoter hidroxidok; a nemfémes ele
mekből a nemiéinek, a savképző oxidok, a savak. Mindegyik vegyület bizonyos reakciók következtében megfelelő sókká alakul.
Az egyszerű anyagok reagálnak az oxigénnel, a fémek, aktivitásuktól függően vízzel, savakkal, sókkal. Az aktív nemfémek reagálnak vízzel, lúgokkal, egyes sókkal.
A szervetlen vegyületek között lejátszódó reakciók végbemehetnek a kémiai jelleg változásával és a jelleg változása nélkül is.
261. Keressétek meg a megfelelőséget az oxid képlete és típusa között:
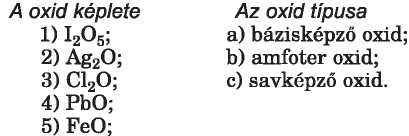
262. Nevezzetek meg két olyan savképző oxidot, melyeknek vízzel való reakciója megfordítható folyamat. írjátok fel a megfelelő reakcióegyenleteket.
263. Állítsátok össze és írjátok le az összes reakcióegyenletet, ami az alábbi oxidok között végbemehet:
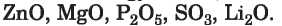
264. Milyen körülmények között megy végbe a nátrium-klorid és a kénsav közötti reakció? Válaszotokat indokoljátok és írjátok fel a megfelelő reakcióegyenletet.
265. A salétromsav reakcióba lép a bárium-karbonáttal, de nem reagál sem a bárium-kloriddal, sem a bárium-szulfáttal. Mivel magyarázható ez a tény? írjátok fel a reakciót molekula- és ionmolekula egyenlettel.
266. Az Ag2S és a NaNO3 sók nem lépnek cserebomlási reakcióba semmilyen más sóval. Mivel magyarázható ez?
267. írjátok fel azokat a reakcióegyenleteket, melyek segítségével meg lehet valósítani az alábbi átalakulási sémákat:
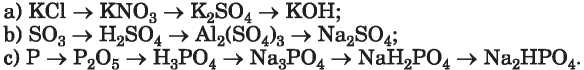
268. 10,7 g ammónium-klorid és megfelelő mennyiségű lúgos oldat reakciójával 4,03 liter ammóniagáz (n.k.k.) keletkezett. Határozzátok meg a reakció termékhozamát.
269. 27,6 g kálium-karbonát és 7,1 g foszfor(V)-oxid keverékét a gázkiválás megszűntéig hevítettek. Mi a reakció szilárd maradéka? Határozzátok meg a maradék összetevőinek tömegszázalékos összetételét.
2. SZÁMÚ GYAKORLATI MUNKA A szervetlen vegyületek közötti származási kapcsolatok
Rendelkezésetekre állnak a következő oldatok: nátriumkarbonát, nátrium-hidroxid, bárium-nitrát, szalmiákszesz, kénsav, valamint az I. változat számára nátrium-hidrogén-karbonát és alumínium-klorid, a II. változat számára nátri-um-tetrahidroxo-aluminát és vas(III)-klorid; ezen felül kémcsőtartó kémcsövekkel, pipetta.
Végezzétek el a tanár által kijelölt feladatokat.
I. VÁLTOZAT
1. feladat. Válasszatok reagenseket (a kiadott vegyszerek közül) és végezzétek el azokat a reakciókat, melyek segítségével meg lehet valósítani a szén vegyületeinek átalakítási sémáját:
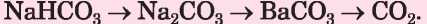
2. feladat. A rendelkezésetekre álló vegyszerek segítségével állítsatok elő alumínium-kloridból alumínium-hidroxidot (többféle módon).
II. VÁLTOZAT
1. feladat. Válasszatok reagenseket (a kiadott vegyszerek közül) és végezzétek el azokat a reakciókat, melyek segítségével meg lehet valósítani az alumínium vegyületeinek átalakítási sémáját:
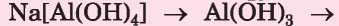
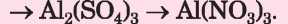
2. feladat. A rendelkezésetekre álló vegyszerek segítségével állítsatok elő vas(III)-kloridból vas(III)-hidroxi-dot (többféle módon).
A munka megkezdése előtt gondoljátok át az egyes feladatokkal kapcsolatos műveleteket, és készítsetek kísérleti tervet: az 1. feladatban például az átalakítási vázlaton lévő nyilak fölé írjátok oda a reagensek képletét.
Készítsetek jegyzőkönyvet: a munka menetét, a megfigyeléseket, a következtetéseket és a reakcióegyenleteket molekuláris alakban, valamint ion-molekula formájában írjátok be a táblázat megfelelő oszlopába:

270. Az I. változat I. feladatában melyik átalakítást lehet elvégezni vegyszerek nélkül? írjátok fel a megfelelő reakcióegyenletet.
271. Milyen reagenst kellene a nátrium-hidrogénkarbonáthoz adni, hogy bárium-karbonát keletkezzen? írjátok fel a reakcióegyenletet.
272. Hogyan lehet az alumínium-nitrátból egyetlen reakció segítségével alumínium-szulfátot előállítani? írjátok fel a megfelelő reakcióegyenletet, jelöljétek a körülményeket.
273. Lehet-e nátrium-tetrahidroxi-aluminát részvételével olyan reakciót végezni, ahol a reakciótermék alumínium-nitrát lesz. írjátok fel a megfelelő reakcióegyenletet molekuláris és ionmolekula formájában.
274. Állítsatok össze kísérleti tervet az alábbi átalakítási vázlatok megvalósításához:
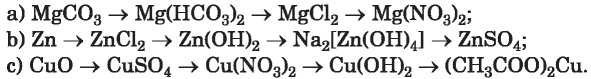
A vázlaton lévő nyilak fölé írjátok oda a reagensek képletét, és írjátok fel a reakcióegyenleteket molekuláris és ion-molekula formájában.
5.
rész
A kémia és az emberiség fejlődése
Az anyagok világában élünk. Egyre újabb és újabb anyagokat állítanak elő, így számuk feltartóztathatatlanul növekszik. Az új anyagok és a belőlük készített eszközök előnyös tulajdonságaik miatt fokozatosan kiszorítják a korábbiakat.
Az ipar, az energetika, a közlekedés fejlődésével, a fogyasztás növekedése folytán egyre több ipari és háztartási hulladék kerül a környezetbe. A hulladékok megbontják a környezet egyensúlyát, károsítják az élő szervezeteket.
Ebben a részben a kémia szemüvegén át vizsgáljuk meg az emberi civilizáció fejlődésének pozitív és negatív irányzatát. Tudomást szereztek arról, mit kell tennie az emberiségnek, hogy megóvhassa a környezetet. Egyik legfontosabb lépés - az ökológiai kultúra kialakítása. A környezetvédelem sikere nagymértékben függ a kémiai eredményektől, a természettudományos műveltségtől.
Ez a tankönyv anyaga Kémia a 11. osztály számára Pavlo Popéi
Наступна сторінка: 34. A kémia és a civilizáció fejlődése